 ��������
��������
�������ƣ�����ʧ�ڻ�֢��ȷ�з��������Բ���ȷ�������ȱ���������쳣����������Ϊʳ���岿��ʳ������Լ�����в�ͬ�̶ȵļ����Բ�����ڡ�Auerbach���ڵ���ϸ������������ϸ��Ϊ��ά��֯���������������Wallerian���ԣ����˶�����ɥʧ��ϸ���塣ʳ��ƽ�����ڹ⾵�����������ڵ羵�±���Ϊ˿�Ա���Ĥ���估ϸ��ή��������Щ�仯��ԭ����̷������������֮������֯ѧ�����ṹ��ҩ��ѧ�о��Ľ����ʾʧ�ڻ�֢��ʳ����ʧ��֧�䡣����λ���Ըɡ���������ά��Auerbach�Լ���������ά�������ܳ���ԭ�������ںδ������������������������Ա������������Ӱ���˴��Ե�����ά��������ϵͳ��
����ʧ�ڻ��IJ��������������£�
1.��ԭ�Բ��� ����ʳ�ܼ�����(Auerbach��)��ϸ�����١�ȱ�硢�����Ա䡢����ά���������ı�����ʾ��Դ�����䡣����ʳ���岿��LES���ļ�������������ˮƽ�Ĵ̼���Ӧ������������ֱ������������������Ӧ�����б�������ʳ�ܶԵ����ܼ���ǿ��Ӧ�ԣ�������ǿ�ҽڶ�������������Cannon���ɣ���ʧȥ��������֯�Ը��������ʵķ�Ӧ�����У�˵��������Ҫ����
2.��������Ԫ���� LES�������˷���(������)��������(�ǵ����ܷ�����������NANC)���֡�Ѫ�ܻ��Գ���(VIP)��һ������(NO)��NANC���������ʣ��鵼ƽ�������š�����ʧ�ڻ�����ʳ���¶�VIP��NO������ά���Լ��١�����������(CCK)�Ի���LES���쳣��������Ҳ��ʾ�����������𡣴��⣬����LES��Ƭ�ĵ�ҩ��ķ�Ӧ��ͬ�ڳ��ˣ�Ҳ��ʾ����ϸ��������쳣��
3.���������쳣 ��֢���������Ե�θ������ϰ������������г�����֢״���ƣ���ʾ��ȥ���������ϰ���
���Ͽ�֪�������������༰ʳ�ܱ��Բ��䡢����������ȱ����ʳ��ȥ����ή�������������ϰ������ص���LES��Ϣѹ���ߣ�����ʱLES�ɳڲ�ȫ����ȫ�����ɳڣ�ʳ���岿ʧ�䶯���˶���Э������ʳ�����ƶ����á�ʹʳ��������ʳ���ڣ���ʳ����ѹ����LESѹ��ʱ�������������ã�����ʳ����ܻ���ͨ�������ڵ�ʳ�����������������ʳ�����š��ӳ���������ʳ����֢������䡣�����о�������Щ���������ƽ��LES�����ʳ���ֳ����䶯������������Ϊʳ���岿���䶯����������ԭ���ԣ�������LES�����йء�
ʧ�ڻ�֢�ۼ���������ʳ�ܣ����������������Ų�����ʼʱʳ�ܽ���ѧ���������Ժ�ʺ����ţ���ʧȥ�����䶯��������Լ��ʺ����ţ���ʧȥ�����䶯��������Լ�������ɳڣ��쳣��Ҫ�����ڲ㻷�м�����������м�������������ʳ��ǻ���ŵij̶ȷ��ᡢ�С���3�ȡ�����ȣ�ʳ��ǻ���������Ż����Ž�����ʳ���¶Σ�һ���ǻ��ֱ����4cm�����������ʳ�PҺ��������ʳ�ܿɼ��ƶ������������жȣ�ʳ��ǻ�������ԣ���ǻ��ֱ����6cm���н϶��ʳ�PҺ��������ʳ���ټ��ƶ������������ضȣ�ʳ��ǻ�������ţ�ǻ��ֱ����6cm���д�����ʳ�PҺ��������ʳ�ܼ������ƶ���������
 �������
�������
������ϣ�
1.����ʧ�ڻ�֢ ������
��������֢״��X���ʳ���岿�����ţ�Զ����Լ�������ɳڣ���ѹ��X�������䶯�����������������ʳ�ܽӺϲ����Ĥ�²㼰�������н����Բ�����ڵļ����������ԭ����θ�����������ټ��������ܰ������������䣬�ΰ���ɷ������Ƶ������ھ������δ��Ԥ�����ţ��öβ��ܽ���еͨ������Ϊ���䲿λ��Ӳ�����������»���ȷ���ʱ��̽����ܿ϶���ϡ�
2.���䶯���쳣 ӲƤ֢�����ʳ��Զ��һ�����䶯�������������ѡ���ʳ�����۳�����Ƥ�����֡�ʳ�ܲ�ѹ����ʳ�ܽ��˳������ۣ���ʳ���岿�䶯�����٣�Զ����Լ���������������ɳ����������䶯�Թ����쳣����ڰ��е���Χ�������м������緢����
���������Ӳ��֢�IJ��ˡ�
3.�������жϺ��
�������� ���ػ�;���ж��������ܷ���
��������������ѡ�����������ж�����Լ75%�IJ��˿ɷ�����ʱ��
������������������������6��֢״��������ʧ��X����ѹ����У��ɼ���ʳ��Զ����Լ�������ɳڼ�żȻ���䶯����������Ҫ���ż�������ơ����ݲ�ʷ���Լ���
4.����ʳ�� ��������ʳ���˶������������������ٵ������Ա���ʳ���ϵı��֡�������������ڲ�ѹ����з���ʳ���˶����ܲ�����ԭ���Լ��̷����䶯�����ϰ������ʺ��
�Է��ľ����������䶯��������ʳ���¶���Լ���ɳڵĴ������ٻ��֣���ʳ���ھ�ֹѹ�����ӡ�
5.Chagas�� �����о�ʳ�ܣ�Ϊ�����ֲ����е�������ļ�������ͬʱ�ۼ�ȫ�����١����ٴ�������ʧ�ڻ�֢�����������ڼ̷��ڼ������Ⱦʹ�������˻���������ѧ��ҩ��ѧ�����Ʒ�Ӧ����ԭ����ʧ�ڻ�֢���ơ�Chagas����ʳ�ܲ����⣬������������ĸı䡣���ǰ����ȷ�����������������ϷǾ�ס������ӫ�����������������ȷ��
�没�Ĺ�ȥ��Ⱦʷ��
6.ʳ�ܡ����Ű� ����ʧ��֢��LES�����ɳڣ�������ʳ���¶˽��ղ����ţ�����ʳ���Ĥ�������쳣��ʳ���¶˼����űڱ����������ã�����ھ�ͨ�������������⣬����˳������θǻ��ʳ�����Ű���ɵ���խ�����ڰ���֯����ܱ����£��Ĥ���ƻ������γ�������ȸı䣬������Թܱڵ�һ��Ϊ������խ���������Բ�ھ�ͨ�������ϴ���խ�����ߣ�����ͨ����ǿ���徵����ɴ��ס�
 ����
����
���ƣ�����ʧ�ڻ�֢��Ŀ�����ɽ�ʳ������Լ�����ɳڷ����Ĺ��裬�Ը���ʳ���ſա�û���κ��ڡ���Ʒ����������˲����������Ƶķ���Ӧ��Ϊ�ǹ�Ϣ�Ʒ��������ڿ�����Ӧ��ƽ�������Ƽ�������������ǿ��ǣ�죬������ʳ�ܼ����п������ж�ʳ�ܵĻ��μ���
1.�ڿ����� ҩ�����Ƶ�Ч���������̣��������룬����ǰ�����ܾ�������������������������ߣ�������һЩ���á����������Ƽ��ܽ�����Լ��ѹ��������ʳ���ſգ������ٴ�Ӧ����Ч���������룬
������ɽ����(
����ʹ)��������ƽ(��ʹ��)�ܽ���ʳ������Լ����������������������ѣ�ijЩ������Σ���˿����á�
2.�������� �ʺ��ڲ������估�����������������������ƵIJ��ˣ�Ҳ����Ϊ���ڴ���������ʧ�������������ƣ���Ϊ����Ч���̣��������ţ��ֶ౻�������ƴ��档ʹ�����ŵ���е�л�е����ˮ�ҡ����Ҽ����ҡ�����ǰϦ���ڼ��ǰ��Сʱ�����˽�ʳ��ʳ�����в�����Ӧ��������ϴ��࣬�����ʳ�ܾ������������š����������Ӽ����ʩ�У����Ų����õ�ˮ�ҡ����һ���ʹʳ��θ���粿������4cmֱ�����ҡ�ǿ�����ŷ����IJ���֢�������ع�����ʹ��ʳ�ܴ��ס���Ѫ������֧����������θʳ�ܷ��������ڷ���ʳ���ס�
3.�������� ����������Ч�������ԣ�ʳ�����ż��������ԣ����������������Ѳ���Σ�գ��ϲ����������ı����������ҡ��ѿ����ɰ��ף���������������ʧ�ܻ������ף����Ĥ���ˣ�����θʳ�ܷ���������ʳ���ף���Ӧ�����������ơ�֢״���ض���Ը��ʳ�����ţ����ʩ�������Ը���֢״��
��������ʧ�ڻ�֢�����кܶ�������������Щ����������խ�����ʳ�ܡ����������ӳ���ʳ�ܡ���������ʳ��θ��ϲ���ʳ��θ�����г��Ǻϻ�ת���������г����г����ŵij�������ʳ�ܼ����п�����ʳ�ܼ����п���������һ�ָ���������ɹ����㷺������ʧ�ڻ�֢��������1913��Heller��1��ʩ��ʳ��ǰ��������п���ʹʳ��˳��ͨ�����Ժ�Zaaijer(1913)��Groeneveldt(1918)�������п�ǰ�ڼ������ͬ��Ч����Ŀǰ�����ô˸������������ɾ�������ǻ;�����С���Ϊ��������θʳ�ܷ�����ʳ�����䲢��֢����������һЩ�Ľ�������������ʳ�ܼ����п�������ʳ��Զ�ˣ�ʳ�ܼ����п����ϲ�Belsey��Nissen��������������ϲ�Thalθ�׳�������ʳ�ܼ����п����������������ʳ��θ�̶������ɾ��ز���;��ʩ�С�һ����Ϊ����;���Ϻã��������꼰�������ˣ�����;��Σ���Խ�С�Ͳ�����죬����ͬʱ�����������г��������һ����ѿ��ޣ���ͬʱ�������������ߣ�Ӧ���ز�;����
���õ����������У�
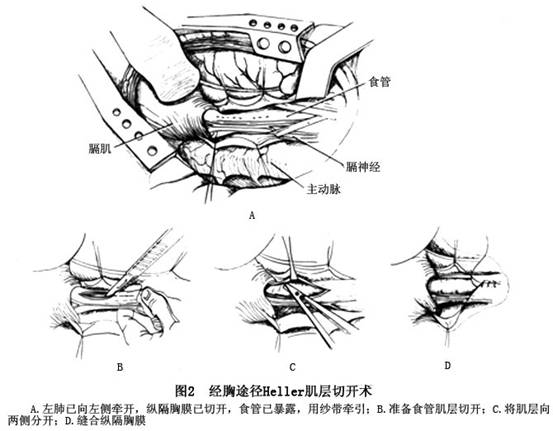
(1)����;��ʳ�ܼ����п���(ͼ2)���Ҳ���λ����������пڿ��أ��Ե�7����г���7�����ߴ����أ�������ǰ��ǣ�����ж��·��ʹ�ֱ���·ξ����������п��ݸ���Ĥ����¶ʳ�ܣ���ɴ������ע�Ᵽ����������ʳ��θ�Ӻϲ�һС����������������Ҫ���������������������ж�ʳ���ѿĸ��Ų��������ܽ�ʳ��θ�Ӻϲ�������ǻ�������ѿ�ǰ����һ���п����ṩ��Ҫ�ı�¶��֮����п�Ӧ�Բ����շ���Ϸ������
��������ʳ�ܣ�Ĵָ��ǰ����Բ�е�Ƭ��ʳ��ǰ��С����һС�пڣ��ö�ͷֱ��ǯ����������μ��������п�С�������Ĥ�²㣬�Զ�ͷ���ӳ������пڣ��������ξ���ˮƽ��Զ����ʳ��θ�Ӻϲ���θ����5��10mm�������п���ɺ��п���Ե�������1/2�ܾ���ʹ�����Ĥ���пڴ������������ȷ������������֮����ϸ���뼡��������Ҫ�жϻ��μ���ע��ֹѪ�������õ��ӻ������������ָѹ��ֹѪ��Ϊ����Ĥ�������ԣ�������ʦ��Ԥ����ʳ��ǻ��֮��θ�����������п�ˮƽ����ɴ������������˹�ǻ������ʦ�����ע�������ѹθ�壬�۲����������θҺ��ʳ�ܼ����п������ݣ������������ݣ�Ӧ��ϸ�߷������ȷ�ϳ��ֹѪ���Ĥ������ʳ�ܷŻ��ݸ����ڼ�������������λ�á��������ѿ��ޣ��ɲ��������ѿ��ؽ������������ǰ��θ���ͽ�θ�ڡ��ݸ���Ĥ�ɲ��ַ���϶��п�����ϡ�����ǻ�����ܺ��ء�
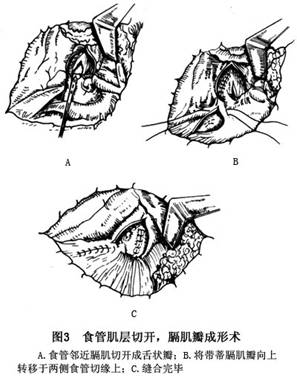
ԭHellerʳ�ܼ����п������Ĥ��������踲�ǣ��Ժ�����˲�ͬ�ĸ���ʽ��Pe-trovsky���������������(ͼ3)��
(2)����ʳ�ܼ����п���ͬʱ�п�������������ǰ����������̽��ʳ�ܡ��Ӻ��ݸ�������ʳ�ܣ�ע�ⲻҪ����Բ���Ĥǻ����������������ˮƽ���������ʳ�ܣ������ж���������ʳ�ܵļ�֧��֧Ѫ�ܡ���ɴ���ƹ���ʳ�ܽ��ˣ�ʹǰ��ʳ��Ĥ���������ж�θʳ�ܽӺϲ����ѿ��Ŵ����������ж�θ��������֧�����¶����ķ�֧������θʳ�ܽӺϲ�������θ��������ǻ���г�λ��θʳ�ܽӺϲ���֬���棬ע�Ᵽ����������θʳ�ܽӺϲ��Ϸ���������ʳ�ܼ����п�����������
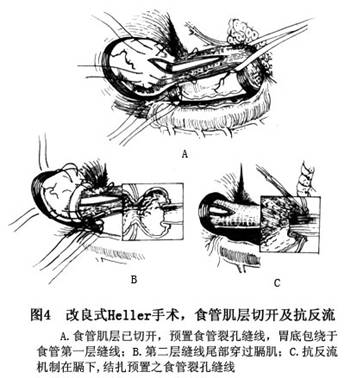
����������Belsey Mark ����������������(ͼ4)��
ʳ�ܼ����пڱ�Ե��θ���̶����ѿ���Ӧ����Է����γɡ�
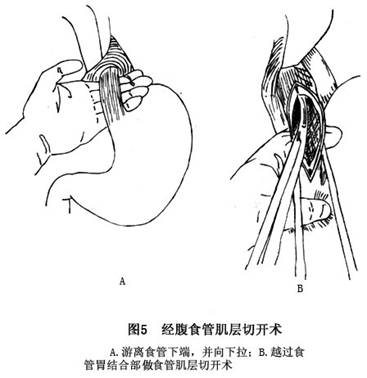
(3)����ʳ�ܼ����п���(ͼ5)��
��������λ���ϸ������пڣ��Խ�ͻ����ˮƽ�����������пڡ���鸹ǻ��¶ʳ�ܽӺϲ���������Ҷ�����·�ǣ�����ж������ʹ����ж�������θʳ�ܽӺϲ��ĸ�Ĥ���ۣ���ʳ�ܶ�������ʳ����Χ����ʳ��Զ����һɴ����¶θʳ�ܽӺϲ���խ������ʱ���ж��������ܽ�ʳ�����¡��漴ʩ��ʳ�ܼ����п����������Ĥ�������ԡ������������������պϸ�ǻ���������ܣ�θ������48h������ʳ�ܼ����п������θ��������ʳ�ܺ��ѿ��������4���˿�ߣ���ǯ��ס���ߣ��Ȳ����ֱ��������ಿ�ֵ��ؽ�����ʳ��θ����֮����2cm����2������ʽ���ߣ��ܿ������п���λ����õڶ����ߺ���������ȥ����ʣ���ٴ��Ϸ��봩���������ࡣ�����߷�ú��ַ������������Ʒ������£����������ߣ����������½�����ʹ�ؽ���λ���������¡�Ȼ������ѿķ��ߡ��ѿ�ҲҪ�����㹻ͨ��һָ���Ŀռ䡣
����Nissen�������ʽ��θ���۵�����Ϊ����θ�ף���ʱ��������жϼ�֧θ�̶�������θ����ʳ�ܺ�����ǰ����Է�ϣ����̶��ڼ����п�֮�¶ˡ�Ϊ����ԭNissen����360������������ʲ����ĺ�����������ְ�����(ͼ6)�����ʳ�ܼ����п���������θ�ײ�����θǰ�ڽ�������ʳ�ܼ��������Ե���Ҳ���Ե��θ�������ϣ�θ��ǰ����ȫ����ʳ�����֮�Ĥ��θ�����²����������̶�����(ͼ7)��
(4)����ʳ�ܼ����п��������������������ʳ�ܼ����п����������ҽ���ʳ�ܺ���0�ŷ��߷��3���4�롣��ʩ��Nissenθ�ײ��۵�����Ӧ��ʳ��ǻ��ͨ��ԼF50��������������ɴ�������θ����������Ӧ�������õ�������������һָͨ����θ��ʳ��Զ�����۵�����θ��ǰ�����ʳ���Ҳ�ڷ��3���4�룬���Ƶij���Ӧ����3cm���������ߺ�ʳ��Զ�˳�360�㱻θ�װ���(ͼ8)���Ա�θ�ܸ���ʳ��������������θ�ڡ���ϸ��ڣ�����������
�����θ�ײ��ְ���������θ�װ���ʳ�ܵ�2/3�ܾ��������������ơ�����ϸ����ǰ������������θ��ǰ����ڷֱ���ʳ���Ҳ�ڹ̶���θ����0-0��˿��Ϸ��Լ5cm���ȡ�
����֢��ʳ�ܼ����п�����֢���٣����������Ĥ���ס�θʳ�ܷ�����ʳ���ѿ���֢״�������
��ʳ���Ĥ���ף���ʳ�ܼ����п���������Ҫ�IJ���֢������ֻҪע��д��ײ���ϸ˿��Ϸ�ϣ����ٷ������⡣����δ��ע����Ĥ�����Ϻ��ַ����Ĵ��ף�������Է���ŧ�ء�������������ȷ�������12h�����ߣ������ٴ�����������������ǻ��ʽ������С��©�ڣ������ڽ�ʳ������Ӫ��֧�ֺ��ڼ����ڿ������ϡ��ϴ�����ڳ���1���������ߣ�������������ʳ���ؽ���
��θʳ�ܷ�����������ʳ���ף�ʳ�ܼ����п�������θʳ�ܷ����ķ����ʺ���ȷ�������ұ�������һ�¡��б�����X��Ƭ�������������ʿɴ�30%��50%��������һ������֢״��������ʳ���ס�����������ʳ����ɳ������ز�ͬ���عǺ���ʹ���ϸ������ƸС��ڿƶ�֢���ƿ��Եõ����⡣�ѷ�����խ�߿��������������������ٴ��������ơ�Ԥ����ʩӦ�ڼ����п�����ʩ��ǡ���Ŀ���������������֢״������֢�������Լ��١�
��ʳ���ѿ��ޣ�Hellerʳ�ܼ����п�����ɲ���ʳ���ѿ��ޡ����Ϳ����ǻ����͡�ʳ�����ͻ����͡�����������θʳ�ܷ�����ʳ����������ɽ�խ�������ѿṹ����֧����֯��ƻ�������ѹ�ı仯ʹ������֯�����ػ��������ڼ����п���ʱ�ѿ��Ų������жϣ��������ؽ�����ͬʱʩ�п�������ʩ���������ʿ��Լ��١�
��֢״�������ʳ�ܼ����п������ֲ����Գ������������ѣ�������Ϊ�����п�����ȫ���п�̫�����£�����45��50F̽����ʳ�����������Խ��֢״�������п����п�����������������ʻ����ߣ���������̫���йأ������������ƣ����ɻ��⡣����һ��֢״ʱ�ں��ַ���֢״�ߣ���ԭ�����Ϊ��
A.������Ե���벻������Ѫ������ʹ��Ե���ϡ�
B.�������������ż�������ʳ�ܡ�
C.��֢״��θʳ�ܷ���������խ��
D.ʳ�ܻ�θ���˷�����֢��
Ӧ�۵�ȷ��֢״������ԭ��Ӧ�����б���������Ч�ߣ�Ӧ����������ơ�������ʽ��ѡ������ڲ��˵������ʧ�ܵ�ԭ�����з��֡��������п�����ֻ������ϣ������ӳ��пڻ������µļ����п���������������խ�����г����ý᳦��ֲ������θ��г���θ���˼�Roux-en-Yθ�ճ��Ǻ����ؽ��������š�����ʳ�ܷ�����֢״����г�ʳ����θ��˳�䶯�᳦�ؽ���



 ���в�ѧ
���в�ѧ
 ����
����
 ��������
��������
 �ٴ�����
�ٴ�����
 ����֢
����֢
 ʵ���Ҽ��
ʵ���Ҽ��
 �����������
�����������

 ���
���
 �������
�������
 ����
����



 Ԥ��
Ԥ��
 Ԥ��
Ԥ��